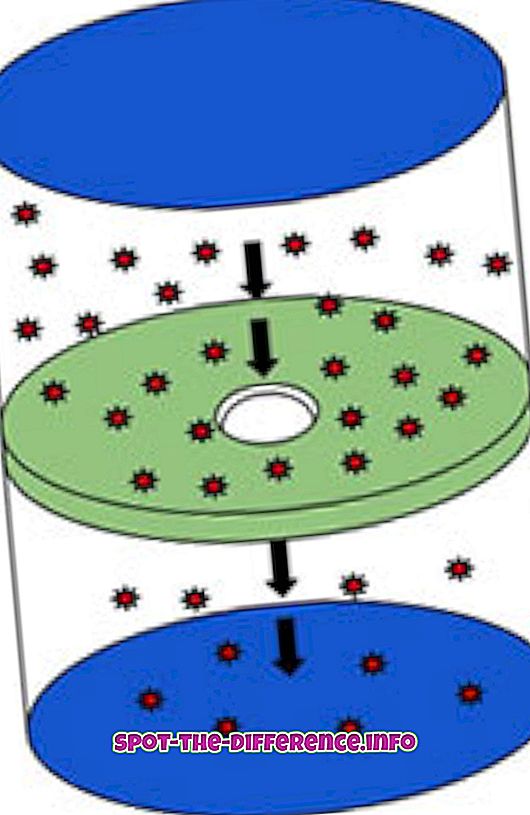
Kluczowa różnica: Dyfuzja to proces, w którym cząsteczki poruszają się i przemieszczają się z jednego miejsca do drugiego bez konieczności masowego ruchu. Efusion jest procesem, w którym cząsteczki przemieszczają się przez otworek z miejsca o wysokim stężeniu do niskiego stężenia.
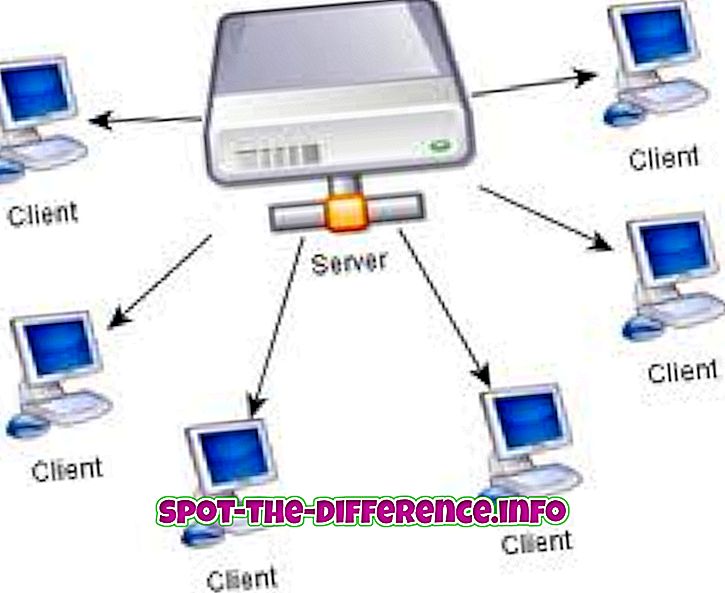
Terminy dyfuzja i wysięk są powszechnie stosowane w wielu naukach, takich jak chemia, fizyka i biologia. W chemii te dwa pojęcia są dwiema właściwościami gazów. Te dwa są mylące dla wielu osób, które dopiero poznają podstawy gazów i ich właściwości. Diffusion i Effusion to dwa różne terminy, które oznaczają dwie różne rzeczy i nie powinny być używane zamiennie. Dyfuzja odnosi się do zdolności gazów do mieszania się ze sobą, podczas gdy wysięk oznacza zdolność gazu do przemieszczania się przez mały otwór. Dyfuzja jest również wykorzystywana w socjologii, ekonomii i finansach w celu odniesienia się do rozpowszechniania ludzi, idei i wartości.
Dyfuzja to proces, w którym cząsteczki poruszają się i przemieszczają się z jednego miejsca do drugiego bez konieczności masowego ruchu. W wyniku dyfuzji cząsteczki poruszają się lub mieszają tylko przy użyciu energii kinetycznej. Słowo "dyfuzja" wywodzi się od łacińskiego słowa "diffundere" oznaczającego "rozprzestrzenianie się". W dyfuzji cząsteczki są w stałym stanie ruchu, a kiedy są napędzane przez energię kinetyczną lub cieplną, mają skłonność do mieszania się z innymi cząsteczkami, co powoduje nierozłączną mieszaninę. Przyjrzyjmy się praktycznemu podejściu, jeden kontener jest podzielony na sekcje A i B za pomocą stałej partycji; pierwsza sekcja jest wypełniona wodą, podczas gdy druga sekcja jest wypełniona czerwonym barwnikiem. Teraz, gdy przegroda zostanie podniesiona, barwnik i woda próbują napełnić cały pojemnik. Następnie barwnik powoli zabarwia wodę na czerwono, co jest dyfuzją.
Dyfuzja powoduje przejście molekuł z obszaru o wyższym stężeniu w obszar o niższym stężeniu, co powoduje mieszanie wszystkich cząsteczek. Dyfuzja zatrzymuje się, gdy wszystkie cząsteczki są równomiernie rozłożone. Dyfuzja nie ogranicza się do wody i działa najlepiej w stanach gazowych, gdzie cząsteczki mają więcej energii i zdolności do mieszania się z innymi cząsteczkami. Istnieją dwa podejścia do dyfuzji: fenomenologiczne i atomistyczne. Zgodnie z podejściem fenomenologicznym cząsteczki przemieszczają się z regionów o wyższym stężeniu do regionów o niższym stężeniu. W podejściu atomistycznym uważa się, że dyfuzja odbywa się w wyniku losowego chodzenia cząstek dyfuzyjnych, w których dyfuzja jest napędzana energią cieplną, powodując ich mieszanie. Dyfuzja odgrywa ważną rolę w tworzeniu minerałów, składników odżywczych i energii, które są wymagane przez organizm.

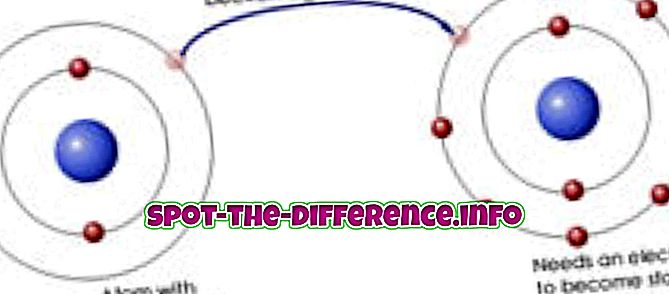
Efusion jest procesem, w którym cząsteczki przemieszczają się przez otworek z miejsca o wysokim stężeniu do niskiego stężenia. Proces opisuje zdolność gazu do przemieszczania się przez mały otwór bez kolizji między cząsteczkami. Dzieje się tak, gdy średnica otworu jest znacznie mniejsza niż średnia swobodna droga cząsteczek. Średnia wolna droga to średnia odległość przemieszczania się cząstki między kolejnymi zderzeniami. Praktycznym przykładem tego byłoby napełnienie pojemnika butelką dymem i włożenie małego otworu do butelki, dym, który zaczyna wydobywać się z otworu, uważany jest za wysyp.
Według szkockiego chemika Thomasa Grahama, który stworzył wzór do mierzenia wysięku, stworzono prawo Grahama, które określa, jak szybko gaz będzie podróżował i jak można go zmierzyć. Zgodnie z prawem Grahama szybkość wydzielania gazów zależy od ich masy cząsteczkowej. Gaz o mniejszej masie cząsteczkowej wypłynie szybciej niż gaz o wyższej masie cząsteczkowej. Efuzję oblicza się, mierząc ile cząsteczek przechodzi przez otwór w ciągu sekundy. Podobnie w termodynamice szybkość wysięku gazu jest odwrotnie proporcjonalna do pierwiastka kwadratowego masy jego cząstek.