Kluczowa różnica: Absorpcja jest zjawiskiem masowym, w którym absorbent całkowicie penetruje ciało stałe lub płyn, tworząc związek lub roztwór. Z drugiej strony, adsorpcja jest zjawiskiem powierzchniowym, w którym cząsteczki adsorbatu koncentrują się tylko na powierzchni adsorbentu.
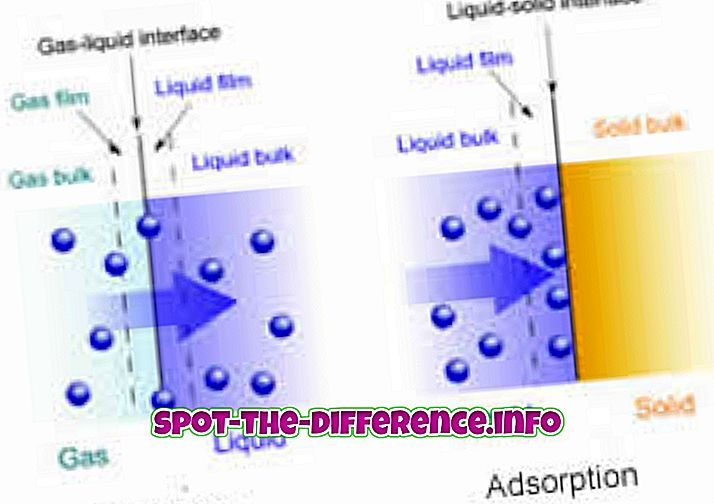
Reakcja chemiczna - dwutlenek węgla pochłaniany przez roztwór węgla potasowego
Proces fizyczny - powietrze wchłaniane w wodzie przez rozpuszczanie

Istnieją dwa rodzaje trybów adsorpcji - chemiczne i fizyczne. W adsorpcji chemicznej cząsteczki i powierzchnia są związane słabymi siłami Vander Walls. Z drugiej strony w adsorpcji chemicznej tworzy się wiązanie chemiczne między cząsteczkami a powierzchnią.
Dlatego główna różnica między adsorpcją i absorpcją polega na tym, że absorpcja jest zjawiskiem masowym, co oznacza, że dzieje się to w całym ciele materiału, podczas gdy adsorpcja pozostaje zjawiskiem powierzchniowym. Adsorpcja jest zawsze egzotermiczna, podczas gdy absorpcja jest endotermiczna. Sorpcja obejmuje oba procesy absorpcji i adsorpcji.
Porównanie adsorpcji i absorpcji:
Adsorpcja | Wchłanianie | |
Defintion | Nagromadzenie gazu lub ciekłej substancji rozpuszczonej na powierzchni ciała stałego lub cieczy | Dyfuzja substancji do cieczy lub ciała stałego w celu utworzenia roztworu lub związku |
Przykład | Gazy obojętne są adsorbowane na węglu drzewnym. | Sucha gąbka absorbuje wodę |
Wymiana ciepła | Egzotermiczny z wyjątkiem adsorpcji H2 na szkle | Endotermiczny |
Osiągnięcie równowagi | Stosunkowo szybciej | Stosunkowo powoli |
Stężenie | Stężenie na powierzchni adsorbentu jest inne niż w masie | Koncentracja pozostaje taka sama w całym materiale |
Szybkość występowania | Początkowo jest szybki, ale później jego tempo zaczyna spadać | Odbywa się według jednolitej stawki |